
Едкий натрий

Спичка и бумажная трубка, побывавшие в растворе NaOH
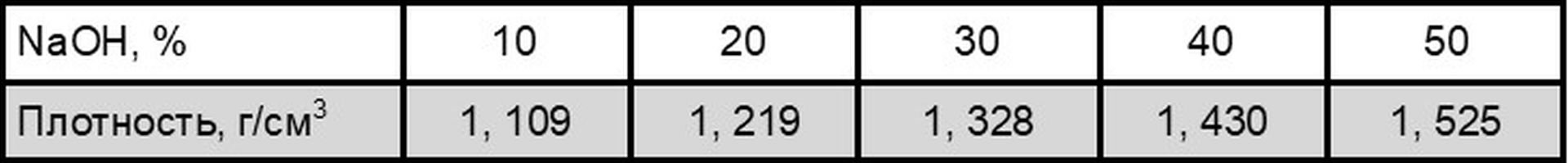
Плотность водных растворов NaOH
Гидроокись натрия (едкий натрий) NaOH — бесцветные кристаллы. При обычной температуре устойчива ромбическая решётка (α-NaOH), а = 3, 397 Å, b = 11, 32 Å, с = 3, 397 Å; выше 299, 6°С превращается в β-NaOH.
Плотность едкого натрия составляет 2, 13 г/см3, температура плавления 320°С, температура кипения 1378°С.
Технический продукт представляет собой белую твёрдую непрозрачную массу с лучистым изломом. Растворимость в воде следующая (в процентах при определённой температуре): 29, 6 (0°С), 52, 2 (20°С), 59, 2 (50°С), 75, 8 (80°С), 83, 9 (192°С). Криогидратная точка –28°С (19% NaOH).
Температура кипения водных растворов различной концентрации следующая (°С): 107, 7 (20% раствор), 128, 0 (40%), 144, 0 (50%).
Известны гидраты едкого натрия, кристаллизующиеся из водных растворов в следующих температурных интервалах:
- NaOH . 7H2O (от –28° до –24°);
- NaOH . 5H2O (от –24° до –17, 7°);
- α-NaOH . 4H2O (от –17, 7° до +5, 4°);
- NaOH . 3, 5H2O (5, 4° - 12, 3°);
- NaOH . H2O (12, 3° - 61, 8°).
Выше 61, 8°C кристаллизуется безводный NaOH.
Гидроокись натрия гигроскопична. При её соприкосновении с водой выделяется большое количество тепла. Водные растворы имеют сильнощелочную реакцию.
Едкий натрий поглощает СО2 из воздуха, превращаясь в карбонат натрия.
В присутствии больших количеств NaOH растворимость солей резко снижается: например, растворимость NaCl в 50%-ном растворе NaOH составляет 0, 91%. Едкий натрий вытесняет также многие органические соединения из их водных растворов, что используют для высушивания органических жидкостей.
Едкий натрий растворим в метиловом (23, 6% NaOH) и этиловом (14, 7% NaOH) спиртах. Практически нерастворим в жидком аммиаке и большинстве органических растворителей. Расплавленная гидроокись натрия растворяет металлический натрий и гидрид натрия. Едкий натрий разрушает кожу, бумагу и другие материалы органического происхождения. На кожу и слизистые оболочки действует прижигающе. Особенно опасно попадание даже малейших его количеств в глаза. Все работы должны производиться в защитных очках и резиновых перчатках.
Получают едкий натрий электрохимическим или химическим способами. Электрохимическое получение основано на электролизе растворов NaCl (получают продукт до 98% NaOH); одновременно получается хлор, а химический способ получения основан на взаимодействии горячего раствора карбоната натрия с известью, в результате которого образуются 10-12% растворы NaOH.